某化学兴趣小组,为了探究Ag、Zn、Cu三种金属活动性顺序,设计了如图所示的四种实验方案,请你判断其中不能达到目的的是( )
- A.
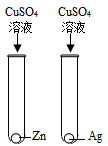
- B.
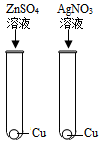
- C.
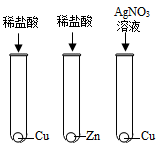
- D.
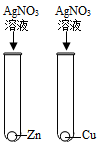
答案
正确答案:D
知识点:金属活动性顺序探究
在金属活动性顺序里,金属的位置越靠前,它的活动性就越强;位于氢前面的金属能置换出盐酸、稀硫酸中的氢;位于前面的金属能把位于后面的金属从它们化合物的溶液里置换出来。
A.Zn能将CuSO4中的Cu置换出来,可观察到Zn的表面有红色物质析出,可得活动性:Zn>Cu;Ag不能将CuSO4中的Cu置换出来,观察不到明显的现象,可得活动性:Cu>Ag。通过现象的对比可判断三种金属的活动性顺序,A能达到目的。
B.Cu不能将ZnSO4中的Zn置换出来,观察不到明显的现象,可得活动性:Zn>Cu;Cu能将AgNO3中的Ag置换出来,可观察到铜的表面有银白色物质析出,可得活动性:Cu>Ag。通过现象的对比可判断三种金属的活动性顺序,B能达到目的。
C.Cu不能和稀盐酸反应,无明显现象,而Zn能和稀盐酸反应,有气泡产生,通过现象对比,可得活动性:Zn>Cu;Cu能将AgNO3中的Ag置换出来,可观察到Cu的表面有银白色物质析出,可得活动性:Cu>Ag。通过现象的对比可判断三种金属的活动性顺序,C能达到目的。
D.Zn和Cu都能将AgNO3中的Ag置换出来,可观察到Zn和Cu的表面均有银白色物质析出,不能判断出Zn和Cu的活动性顺序。D不能达到目的。
故选D。
略







