将50gA物质和10g B物质混合,加热后发生化学反应。经分析,反应后的混合物中含有20gA,含C、D的质量比为11:9。若A、B、C、D的相对分子质量分别为30、20、44、18,则它们之间发生的化学反应可表示为( )
- A.A+B=C+D
- B.A+2B=2C+D
- C.2A+B=2C+D
- D.2A+B=C+2D
答案
正确答案:D
化学方程式xA+yB=zC+kD遵循质量守恒定律,即mA +mB =mC +mD,在化学方程式中,各物质按照一定的质量比参加反应,即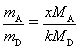 。由
。由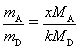 可得,
可得,![]() 。
。
根据题意可知,A、B为反应物,C、D为生成物,可表示为xA+yB=zC+kD。
参加反应的A的质量为50g-20g=30g,B的质量是10g,根据质量守恒定律可知,生成C、D的质量和为40g,因为C、D的质量比为11:9,所以生成C、D的质量分别为22g、18g。
则![]() ,所以化学反应可表示为:
,所以化学反应可表示为:
2A+B=C+2D。
故选D。
略







