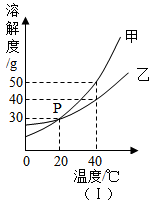
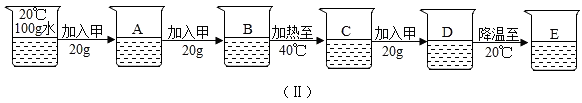
下图(Ⅰ)是甲、乙两种固体物质的溶解度曲线。20℃时,小明进行了如下图(Ⅱ)所示的实验。下列有关说法正确的是( )
- A.20℃时,甲、乙两种物质的溶液中溶质质量分数相等
- B.小明的实验过程中,只有B、D属于饱和溶液
- C.D溶液中溶质质量分数为50%
- D.若向E中加入100 g水,则溶液中溶质的质量分数不变
答案
正确答案:D
知识点:溶解度曲线的应用
由溶解度曲线可知,甲的溶解度随温度的升高而增大,20℃时甲的溶解度为30g,40℃时甲的溶解度为50g。
由图(Ⅱ)可知,20℃时向100g水中加入20g甲,固体能够全部溶解,所得溶液A为不饱和溶液(溶质质量为20g);溶液A继续加入20g甲,固体不能全部溶解,所得溶液B为饱和溶液(溶质质量为30g);溶液B加热至40℃(溶解度增大为50g),固体全部溶解,所得溶液C为不饱和溶液(溶质质量为40g);溶液C继续加入20g甲,固体不能全部溶解,所得溶液D为饱和溶液(溶质质量为50g);溶液D降温至20℃,饱和溶液D中的固体继续析出一部分,所得溶液E为20℃时的饱和溶液(溶质质量为30g)。
A.20℃时,甲、乙两种物质的溶解度相等,则两种物质饱和溶液的溶质质量分数相等,不确定溶液是否饱和,故无法判断两种物质的溶液溶质质量分数的大小关系。A错误。
B.由上述分析可知,B、D、E属于饱和溶液。B错误。
C.D溶液中溶质质量为50 g,溶剂质量为100 g,则溶质质量分数为33.3%。C错误。
D.20℃时甲的溶解度为30g,则200g水中可溶解甲的质量为60g,即前面加入的60g固体甲能够恰好全部溶解,形成20℃时的饱和溶液。未加水前E也为20℃时的饱和溶液,故溶质质量分数不变。D正确。
故选D。
略









