下列对水垢的主要成分是CaCO3和Mg(OH)2而不是CaCO3和MgCO3的原因解释,下列说法正确的有( )
①Mg(OH)2的溶度积大于MgCO3的,且在水中发生了沉淀转化。
②Mg(OH)2比MgCO3更难溶,且在水中发生了沉淀转化。
③MgCO3电离出的CO32-发生水解,使水中OH-浓度增大,对Mg(OH)2的沉淀溶解平衡而言,Q(Mg(OH)2)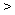 Ksp(Mg(OH)2),生成Mg(OH)2沉淀。
Ksp(Mg(OH)2),生成Mg(OH)2沉淀。
④MgCO3电离出的CO32-发生水解,使水中OH-浓度减小,对Mg(OH)2的沉淀溶解平衡而言,Q(Mg(OH)2)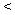 Ksp(Mg(OH)2),生成Mg(OH)2沉淀的是。
Ksp(Mg(OH)2),生成Mg(OH)2沉淀的是。
- A.①③
- B.①②
- C.②③
- D.②④
答案
正确答案:C
知识点:沉淀溶解平衡的应用
①Mg(OH)2的溶度积小于MgCO3的,水中的碳酸氢镁受热分解生成碳酸镁,碳酸镁会继续生成更难溶的氢氧化镁,在水中发生了沉淀转化,故①正确;
②Mg(OH)2比MgCO3更难溶,故②正确;
③MgCO3电离出的CO32-发生水解,使水中OH-浓度增大,使Q(Mg(OH)2)![]() Ksp(Mg(OH)2),生成Mg(OH)2沉淀,故③正确;
Ksp(Mg(OH)2),生成Mg(OH)2沉淀,故③正确;
④MgCO3电离出的CO32-发生水解,使水中OH-浓度增大,故④错误。
故选C。
略







