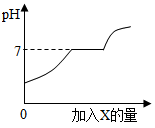
现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH随滴入X的量的变化关系如图所示,则X是( )
- A.水
- B.氯化钠溶液
- C.澄清石灰水
- D.纯碱溶液
答案
正确答案:D
需结合图象的变化和酸碱盐之间的反应进行分析。
随着X的加入溶液由酸性逐渐变为碱性,因此X是一种显碱性的物质,A、B均错误。刚开始加入X时,pH逐渐增大,说明酸性逐渐减弱,故加入的X先和盐酸反应;中间一段pH不发生变化,pH为7,说明X能与CaCl2发生反应且生成在溶液中显中性的物质,澄清石灰水不满足,CaCl2能与Na2CO3反应生成CaCO3沉淀和NaCl,满足题意;当CaCl2消耗完再继续加入Na2CO3溶液,由于Na2CO3溶液显碱性,所以pH值逐渐增大。综上所述,加入的物质为纯碱溶液,
故选D。
略








