用木炭还原氧化铜的实验如图所示:

(1)刚开始预热,试管②中立即产生气泡,但石灰水不变浑浊,原因是什么?
(2)继续加热,观察到石灰水逐渐变浑浊,黑色粉末中出现红色物质,写出发生反应的化学方程式。
(3)停止加热时,应先将导管从试管②中撤出,待试管①冷却后再把试管里的粉末倒出,这样操作的原因是什么?
(4)下课后,同学们仔细观察试管里倒出的粉末,发现红色的粉末中还有一些黑色的粉末混杂,有几位同学推测了黑色粉末的组成情况:①可能是没有反应完的木炭;②可能是没有反应完的氧化铜;③可能是没有反应完的木炭和氧化铜的混合物。请你设计实验证明推测①成立(写出具体的实验步骤、现象及结论)。
(5)实验室可采用木炭还原氧化铁的方法得到铁,计算用含Fe2O360%的赤铁矿石800t,理论上可炼出纯铁多少吨?
答案
(1)刚开始试管内的气体受热膨胀,排出来的是空气(2分)。
(2)C+2CuO![]() 2Cu+CO2↑(2分)。
2Cu+CO2↑(2分)。
(3)将导管从试管②中撤出是为了防止试管②中的液体倒吸进入试管①中造成试管炸裂(2分),冷却后再把试管里的粉末倒出是为了防止铜被空气中的氧气重新氧化(2分)。
(4)取该黑色粉末在空气中充分灼烧(1分),观察到黑色粉末逐渐消失(2分),则证明黑色粉末为木炭(1分)。
(5)解:设理论上可炼出纯铁的质量为x。(1分)
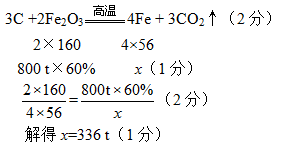
因此,理论上可炼出纯铁336吨。(1分)
(1)刚开始加热时,试管中的空气膨胀逸出,但此时碳和氧化铜未反应,因此观察到的现象是有气泡冒出但石灰水不变浑浊。
(2)继续加热,碳和氧化铜发生反应,反应的化学方程式为C+2CuO![]() 2Cu+CO2↑。
2Cu+CO2↑。
(3)停止加热时,为了防止试管②中的液体倒吸进入试管①中造成试管炸裂,应先将导管从试管②中撤出,为了防止铜被空气中的氧气重新氧化,应先冷却后再把试管里的粉末倒出。
(4)证明猜想①成立,即证明黑色粉末为木炭,可利用木炭的性质进行验证。木炭具有可燃性,在空气中燃烧生成二氧化碳,因此可设计实验为取该黑色粉末在空气中充分灼烧,观察到黑色粉末逐渐消失,则证明黑色粉末为木炭。
(5)解:设理论上可炼出纯铁的质量为x。

因此,理论上可炼出纯铁336吨。
略








