单选题(本大题共小题, 共分)
-
1.(本小题2分)
生活中发生的下列变化,属于化学变化的是( )
-
2.(本小题2分)
燃煤排出的二氧化硫进入大气后,会引起的环境问题是( )
-
3.(本小题2分)
用氯化钠固体配制一定质量分数的氯化钠溶液,不需要用到的仪器是( )
-
4.(本小题2分)
某物质不含碳元素和氢元素,它不可能是( )
①酸②碱③盐④有机物
-
5.(本小题2分)
如图是甲、乙两种固体物质的溶解度曲线,下列说法正确的是( )
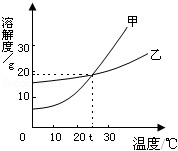
-
6.(本小题2分)
“信阳毛尖”是一种绿茶,绿茶中含有的单宁酸(化学式为C76H52O46)具有抑制血压上升、清热解毒等功效。下列有关单宁酸的说法正确的是( )
-
7.(本小题2分)
有元素化合价升降的反应是氧化还原反应。下列属于氧化还原反应的是( )
-
8.(本小题2分)
下列实验不能达到实验目的的是( )

-
9.(本小题2分)
相同质量的H2、CH4和CO完全燃烧需要氧气的质量( )
-
10.(本小题2分)
能在pH为1的溶液中大量共存,且溶液为无色透明的一组物质是( )
解答题(本大题共小题, 共分)
-
11.(本小题4分)
请从氮气、熟石灰、氧气、硝酸钾中选择适当的物质填空:
可充入食品包装袋中防腐的物质是 ;农业上可作复合肥料的物质是 。
-
12.(本小题4分)
区分某地下水(硬水)和蒸馏水,可以选用的物质是 ;
了解某工厂排放废水的酸碱度,可以使用 进行测定。
-
13.(本小题6分)
“岩盐之都”河南叶县盛产食盐。食盐的主要成分NaCl由 (填“分子”、“原子”或“离子”)构成;除去食盐水中泥沙等不溶性杂质的方法是 ;电解食盐水可制烧碱:2NaCl+2H2O
 2NaOH+H2↑+X↑,则X的化学式为 。
2NaOH+H2↑+X↑,则X的化学式为 。
-
14.(本小题6分)
2011年是“国际化学年”。化学与生活密切相关,合理选择饮食、正确使用药物等都离不开化学。水果、蔬菜能为人体提供的主要营养素是 ;人体缺少必需微量元素会得病,如缺 会引起甲状腺肿大(俗称大脖子病);含小苏打的药物治疗胃酸过多症的化学方程式为 。
-
15.(本小题6分)
一定条件下,下列物质在密闭容器内充分反应,测得反应前后各物质的质量如下:

则反应后A的质量为 ;该反应所属的基本反应类型是 ;该反应中B和D两种物质变化的质量比为 。
-
16.(本小题6分)
在Cu(NO3)2、A1(NO3)3和AgNO3的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤出的固体上滴加稀硫酸时有气泡产生。则反应后所得溶液中含有的金属离子有 ;反应后溶液的质量比原混合溶液的质量 (填“大”或“小”);有关反应的化学方程式为 (写出一个即可)。
-
17.(本小题4分)
如图是某硫酸试剂瓶标签上的部分文字说明。

(1)取10 mL该硫酸可配制成9.8%的硫酸 g。
(2)取适量该硫酸与锌反应可生成SO2气体:Zn+2H2SO4(浓) ZnSO4+SO2↑+2H2O。
ZnSO4+SO2↑+2H2O。
反应一段时间后,还可能生成另一种气体,请解释其原因。
-
18.(本小题6分)
金属是一类重要的材料,其应用十分广泛。
(1)铝的利用比铜和铁晚。金属大规模开发和利用的先后顺序与下列 有关。
甲.金属的活动性乙.金属的导电性丙.金屑在地壳中的含量
(2)相同的铁栏杆,为什么安装在南方沿海地区比安装在北方更容易生锈?
(3)写出用盐酸清洗铁锈(主要成分是Fe2O3)的化学方程式。
-
19.(本小题6分)
如图是实验室制取气体的常用装置。

(1)A中的试管口为什么应略向下倾斜?
(2)写出选用B制取氧气的化学方程式。
(3)若采用C(气体由a口进入)收集到一种气体,请简述验证该气体的实验方法。
-
20.(本小题8分)
氯气(Cl2)是有刺激性气味的有毒气体。氯气可与水反应:Cl2+H2O
 HCl+HClO(次氯酸)。如图是探究物质漂白性(使有色物质退色)的实验。
HCl+HClO(次氯酸)。如图是探究物质漂白性(使有色物质退色)的实验。
(1)闻氯气时,在操作上应注意什么问题?
(2)写出如图C中Cl2与NaOH溶液反应的化学方程式。(提示:HClO+NaOH NaClO+H2O)
NaClO+H2O)
(3)图中实验的现象为:B中布条退色而A中布条不退色,由此可推测具有漂白性的物质可能有哪些?若要证明只有次氯酸有漂白性,还需补做相关的实验,请简要写出实验的步骤和现象。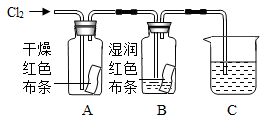
-
21.(本小题24分)
碳是形成化合物种类最多的元素,含碳物质是中学化学研究的重要内容。
(1)“低碳生活”倡导低能量、低消耗,主要是为了减少 (填化学式)的排放量。
(2)如图1为元素周期表中的一格,下列说法不正确的是 (填标号)。
A.碳元素属于非金属元素B.碳原子核内质子数为6
C.碳元素的原子结构示意图为 D.碳的相对原子质量为12.01
D.碳的相对原子质量为12.01
(3)甲、乙、丙、丁是初中化学常见的化合物,甲和乙中含有碳元素,丙能做干燥剂。它们之间有如图2所示的转化关系(部分物质和反应条件已略去)。则甲的化学式为 ;丙转化为丁的化学方程式为 。
(4)图3是某趣味实验装置图。挤压胶头滴管后,可观察到气球胀大的现象。请分析其原因,并写出化学方程式 。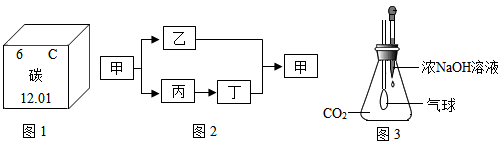
(5)利用下图装置可做CO还原Fe2O3的实验,并检验该反应生成的气体产物。已知由A装置制取的CO气体中混有少量的CO2。
①CO与Fe2O3反应的化学方程式为 。
②气体通过装置的顺序是A→ (装置不能重复使用)。
③从环保角度考虑,对以上装置的改进措施是 。
(6)称取12.5 g石灰石(主要成分是CaCO3,杂质不参加反应)放入烧杯中,向其中加入50 g稀盐酸,二者恰好完全反应。反应结束后称量烧杯中剩余物质的总质量为58.1 g(不包括烧杯的质量,且气体的溶解忽略不计)。试计算石灰石中杂质的质量分数。







